| Главная » Статьи » Физика |
Литиевая батарея и топливные элементы
Для портативных электронных устройств необходимы различные
типы миниатюрных элементов питания и батареек. Аккумуляторы требуются для запуска
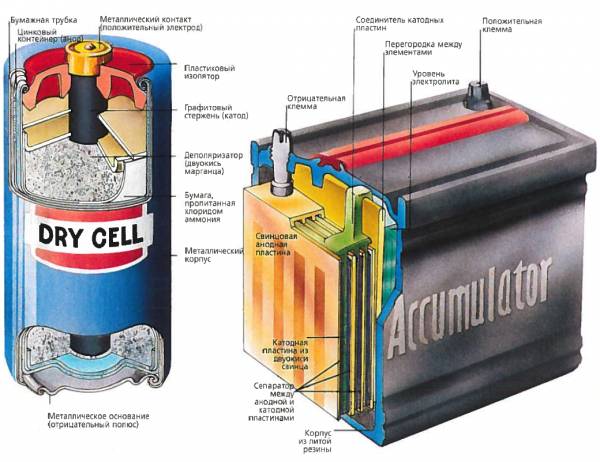
двигателей автомобилей и для питания портативных устройств. (В сухом элементе электроны движутся от анода(цинкового корпуса) к катоду (графитовому стержню). Свинцово-кислотный автомобильный аккумулятор состоит из шести перезаряжаемых двухвольтовых элементов, соединенных последовательно и дающих напряжение 12 В. Каждый элемент состоит из свинцового анода и катода из двуокиси свинца, погруженных в электролит из слабого раствора серной кислоты.)
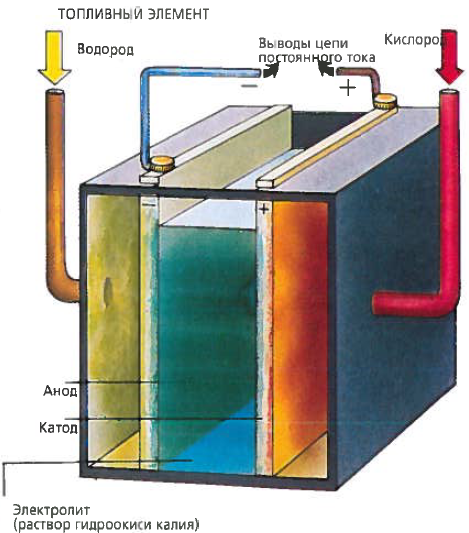
(В водородно-кислородном топливном элементе газы пропускают через пористые никелевые электроды, где в результате реакции образуется вода и электроны, движущиеся по цепи.) Батареи состоят из
нескольких элементов питания, соединенных вместе для получения более высокого
электрического напряжения. Некоторые ошибочно называют элемент питания
батареей. Толчком к изобретению химических источников тока послужила обычная лягушка.
В 1786 г. итальянский физиолог Луиджи Гальвани обнаружил, что вскрытые лягушки
дергаются при прикосновении скальпеля. Затем совершенно случайно он определил,
что лягушечьи лапы могут двигаться просто при соприкосновении с металлом!
(Инструменты, питающиеся от батареек,более удобны, чем работающие от сети. Электрическая отвертка питается от никель-кадмиевых аккумуляторов. для зарядки она вставляется в зарядное устройство, подключаемое к сети.) Ясность в этот вопрос
в 1790 г. внес его соотечественник, физик Алессандро Вольта. Ножки лягушки
дергаются вследствие того, что жидкость внутри них реагирует при контакте с
двумя металлами: латунью II железом. В этом случае образуется простой элемент
(химический источник тока), напряжения которого достаточно, чтобы вызвать
сокращение мышцы лягушки. Вслед за этим Вольта сконструировал элемент, (впоследствии
названный его именем), расположив кусочек мокрой бумаги между пластинами цинка
и меди. Элемент Вольта был очень слабым, но вслед за ним разработал вполне
практичные элементы и батареи. Одна из них состояла из цилиндра, сделанного из цинковых
и медных пластин с бумажным сепаратором, пропитанным раствором соли. Эта
батарея получила название вольтова столба.
(Автомобиль Синклер С5 может двигаться с помощью педалей или электромотора, но энергии его кислотно-свинцового аккумулятора недостаточно для длительных путешествий.) Принцип действия Со времени открытия
Вольта было изобретено много подобных элементов питания. Для электродов и
растворов электролитов использовались различные вещества и материалы. Все эти
элементы действуют за счет преобразования химической энергии в электрическую. Электролит
состоит из ионов (заряженных частиц), которые движутся к электродам. Один
электрод притягивает отрицательно заряженные ноны. Другой — положительно заряженные — катионы. Когда электрическая цепь между электродами замыкается, электроны в элементе начинают двигаться от отрицательного
к положительному полюсы, образуя электрический ток. (Водитель "ритма сердца"работает на пяти ртутныхэлементах длительного действия.Он создает электрические импульсы для работы сердечной мышцы.) Типы элементов питания Первичные элементы
выходят из строя, когда химические вещества внутри прореагировали между собой и
не могут больше давать необходимый ток. Вторичные элементы можно перезаряжать.
Электричество от подходящего зарядного Устройства, обычно питающегося от сети, пропускаю
через подсевший элемент, тем самым восстанавливая химические реагенты в
элементе до первоначального состояния. Электрический заряд, поступающий в элемент,
сохраняется в виде химической энергии, которая накапливается (аккумулируется) в
нем. Поэтому батареи вторичных элементов называют аккумуляторами, их используют
в автомобилях, бытовых и других электрических устройствах.
(Электронные и электрическиесистемы космического кораблямогут работать за счет солнечной энергии, котораяпреобразуется в электрическуюпри помощи солнечных батарей.) Химия элементов питания Самый распространенный гальванический элемент основан на изобретении, сделанном французским ученым Жоржем Лекланше в 1860 г. Он состоит из цинкового корпуса (отрицательный электрод) и диоксида марганца с добавлением графитового стержня (положительный электрод). Хотя этот элемент называется сухим, его электролит является густой пастой хлорида аммония. Во время его работы на графите выделяется водород, который необходимо удалить, так как он понижает эффективность элемента. Для этого используют вещество, называемое деполяризатором, — в данном случае двуокись марганца. Перезаряжаемые батареи в большинстве своем состоят из кислотно-свинцовых элементов, изобретенных в 1860 г. Гастоном Планте. В них электроды из свинца и его двуокиси погружены в слабый раствор серной кислоты. В процессе работы оба электрода покрываются сульфатом свинца. При зарядке они превращаются соответственно в свинец и его двуокись. Перезаряжаемые никель-кадмиевые элементы имеют электроды из гидроксидов никеля и кадмия, погруженные в раствор гидроксида калия. Такие элементы могут заменять первичные сухие, а также используются в некоторых типах фонариков, инструментов и других беспроводных бытовых устройствах. (Большая матрица из солнечных элементов при ярком солнечном свете дает достаточно энергии для движения автомобиля.) Понравилась статья? Тогда советуем ознакомиться со следующими: | |
| Просмотров: 3919 | Теги: | Рейтинг: 0.0/0 |
| Всего комментариев: 0 | |